پنجشنبه 08 اسفند 1404 - 04:05
دانشمندان برای اولین بار تصاویری از استراتژی سرّی سرطان ثبت کردند
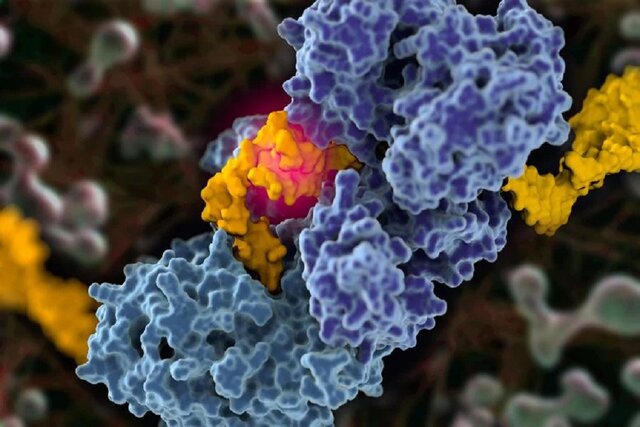
ایسنا/ پروتئینهای ترمیم کننده دیانای به عنوان ویرایشگرهای مولکولی بدن عمل میکنند و به طور مداوم آسیب کد ژنتیکی ما را شناسایی و تصحیح میکنند. یک چالش که برای مدت طولانی محققان را درگیر کرده، درک این موضوع بوده است که چگونه سلولهای سرطانی از یکی از این پروتئینها به نام پلیمراز تتا (Pol-theta) برای حمایت از بقای خود استفاده میکنند. اکنون دانشمندان اولین تصاویر با وضوح بالا از پلیمراز تتا را ثبت کردهاند که نقش آن را در توسعه سرطان روشن میکند.
این مطالعه که در روز ۲۸ فوریه سال ۲۰۲۵ منتشر شده است، نشان میدهد که پلیمراز تتا در هنگام اتصال به رشتههای دیانای شکسته، دچار تحول ساختاری قابل توجهی میشود. این تحقیق با ترسیم وضعیت فعال و متصل به پلیمراز تتای دیانای، پایهای برای طراحی درمانهای دقیقتر و موثرتر سرطان فراهم میکند.
به نقل از استیدی، گابریل لندر (Gabriel Lander)، نویسنده ارشد این مطالعه میگوید: اکنون تصویر واضحتری از نحوه عملکرد پلیمراز تتا داریم که به ما این امکان را میدهد تا فعالیت آن را با دقت بیشتری مسدود کنیم.
پلیمراز تتا: یک بازیکن کلیدی در بقای سلولهای سرطانی
از نظر فنی، پلیمراز تتا یک آنزیم است. نوعی پروتئین که واکنشهای شیمیایی، از جمله واکنشهای مربوط به ترمیم سلول را سرعت میبخشد. آسیب دیانای یک مشکل همیشگی برای سلولها است که میلیونها بار در روز به طور جمعی در سراسر بدن ما رخ میدهد.
سلولها معمولا از مکانیسمهای بسیار دقیقی برای رفع این شکستها استفاده میکنند، اما برخی از سرطانها بهویژه سرطانهایی که از جهشهای BRCA1 یا BRCA2 ناشی میشوند، مانند برخی سرطانهای پستان و تخمدان، این عملکرد را ندارند. در عوض، آنها به روشی مستعد خطا وابسته هستند که توسط پلیمراز تتا کنترل میشود.
کریستوفر زریو (Christopher Zerio)، نویسنده اول این مطالعه، محقق سابق فوق دکترا در آزمایشگاه لندر، میافزاید: پلمراز تتا یک هدف مهم است و بسیاری از شرکتهای داروسازی آن را راهی امیدوارکننده برای درمان سرطانهایی میدانند که مسیرهای ترمیم دیانای معیوب دارند.
اگرچه مطالعات قبلی بخشهایی از ساختار پلیمراز تتا را ترسیم کردهاند، اما تعاملات آنزیم با دیانای به خوبی شناخته نشده بود.
زریو میگوید: آنچه مشخص نشده بود این بود که چگونه پلیمراز تتا واقعا دیانای را درگیر میکند که این برای توسعه دارو ضروری است.
ثبت پلیمراز تتا در لحظه عمل
تحقیقات قبلی نشان داده است که پلمراز تتا به دو شکل وجود دارد: تترامر که شامل چهار نسخه از آنزیم است و دیمر که شامل دو نسخه است. اما چرا یا چگونه پلیمراز تتا بین این اشکال تغییر میکند، ناشناخته بود.
قبل از این مطالعه، ساختار پلیمراز تتا فقط در حالت غیرفعال ثبت شده بود، و یک شکاف علمی بزرگ در مورد نحوه تعامل آنزیم با دیانای باقی مانده بود.
لندر توضیح میدهد: میدانید که تعامل اتفاق میوفتد، اما بدون دیدن آن، این مکانیسم مانند یک راز باقی میماند.
با استفاده از میکروسکوپ الکترونی کرایو و آزمایشهای بیوشیمیایی، این گروه در حین ثبت پلیمراز تتا در لحظه عمل ترمیم دیانای به کشف شگفتانگیزی دست یافتند. هر زمان که پلیمراز تتا به رشتههای شکسته متصل میشد، پیوسته از حالت تترامریک به یک پیکربندی دیمری که پیش از این دیده نشده بود تغییر میکرد.
زمانی که پلیمراز تتا در حالت فعال خود قرار گرفت، دیانای را با استفاده از یک فرآیند دو مرحلهای ترمیم کرد. در مرحله اول، آنزیم دنبالههای منطبق کوچکی به نام «میکروهومولوژیز» (microhomologies) در رشتههای شکسته را جستجو میکند. هنگامی که یک توالی منطبق پیدا شد، پلیمراز تتا رشتههای دیانای شکسته را نزدیک به هم نگه میدارد تا بتوان بدون نیاز به انرژی اضافی به هم وصل شوند. بیشتر آنزیمها برای عملکرد خود به تقویت انرژی نیاز دارند، اما پلیمراز تتا به جاذبه طبیعی بین توالیهای دیانای منطبق تکیه میکند و به آنها اجازه میدهد به خودی خود در جای خود قرار گیرند.
زریو میگوید: اگر بتوانیم این فرآیند را مسدود کنیم، میتوانیم سرطانهای وابسته به پلیمراز تتا را نسبت به درمان حساستر کنیم.
پلیمراز تتا در سطوح پایین در سلولهای سالم تولید میشود و همین آن را به یک هدف امیدوارکننده برای درمان سرطان تبدیل میکند. برخلاف سلولهای سرطانی که به پلیمراز تتا وابسته هستند، سلولهای سالم به مکانیسمهای ترمیم دقیقتری متکی هستند که به انرژی نیاز دارند که ترمیم دقیقتر دیانای را تضمین میکند. از آنجایی که سلولهای سالم برای بقا به پلیمراز تتا نیازی ندارند، مسدود کردن فعالیت آنزیم احتمالا باعث آسیب گسترده به بافت سالم نمیشود.
لندر خاطرنشان میکند: بیشتر داروهای سرطان پروتئینهایی را هدف قرار میدهند که سلولهای سالم نیز به آنها نیاز دارند. به طور خاص هدف قرار دادن پلیمراز تتا فقط باید سلولهای سرطانی را از بین ببرد و احتمال عوارض جانبی در طول درمان را کاهش دهد.
داروهایی که پلیمراز تتا را مهار میکنند در حال حاضر در آزمایشهای بالینی هستند، اما در حال حاضر باید با سایر درمانها ترکیب شوند تا به طور مؤثر عمل کنند. در حالی که این مطالعه میتواند به توسعه داروی دقیقتری کمک کند، تحقیقات بیشتر ممکن است نقشهای دیگری را که آنزیم ممکن است در عملکردهای سلولی ایفا کند نشان دهد.
پربیننده ترین
-
عکس مسی درآمد؛ آخرین توپ طلا با آرایشگر ویژه!
-
10 جایزه 5 میلیون تومانی برای کاربران آخرین خبر (مهلت شرکت در مسابقه تا 9 آذر تمدید شد.)
-
10 جایزه 5 میلیون تومانی برای کاربران آخرین خبر (مهلت شرکت در مسابقه تا 9 آذر تمدید شد.)
-
چراغ قوه همه کاره ( پاور بانک، شیشه شکن و ... )
-
هشدار آبفای کشور به مردم؛ هیچ ماموری فعلا برای قرائت کنتور آب مراجعه نمیکند
-
آخرین وضعیت راهها در چهارمین روز از سال جدید؛ محور چالوس از شنبه دوباره بسته میشود
-
جارو شارژی !! دیگه نگران نظافت ماشین نباشید
-
زنده؛ بیرانوند در یک قدمی استقلال
-
"دنا پلاس اتومات" بخریم یا "تارا اتومات؟"/ مقایسه اختصاصی "آخرینخودرو" از دو خودروی پرطرفدار
-
فشار آبرو چند برابر کن ....
-
فرمانده کل قوا: ملت ایران در مقابل جنگ تحمیلی محکم میایستد همانگونه که در مقابل صلح تحمیلی نیز محکم خواهد ایستاد
-
چالش/ بازیکن داخل تصویر رو حدس بزن (16)
-
5 نشانه ضعیف شدن ریه ها و بهترین روش تقویت آن چیست؟
-
لندکروزر یا ۲۰۶؟ / مقایسه جالب "آخرینخودرو" به بهانه سخنان جنجالی میرسلیم
-
پایان زودهنگام گنبد آهنین؟ اسرائیل مجبور به جیرهبندی موشکها شد
-
سپ، برترین شرکت در خاورمیانه شد
-
گردونه را بچرخانید، بیتکوین دریافت کنید
-
واکنش عراقچی به تجاوز امروز آمریکا به تأسیسات هستهای فردو، نطنز و اصفهان
آخرین اخبار
-
دهنمکی: ماجرای مهسا امینی را پیشبینی کرده بودم!
-
ویدئویی از بازیگری کارگردان «سووشون» در یک مستند
-
وقتی خورشید زبانه میکشد
-
واکنش رئیس رسانه ملی به انتقادات از اظهارات برخی کارشناسان صداوسیما
-
پاسخ کوبنده دختر محمود نقاشِ «پایتخت» به بیحرمتی به شاهنامه
-
کپسول «دراگون» به ایستگاه فضایی بینالمللی متصل شد
-
علت ماندگاری نام استاد فرشچیان از زبان اسماعیل آذر
-
سیاوش خیرابی خطاب به شاهرخ استخری: نمیگم اونموقعها با هم کجاها میرفتیم
-
یه سوت بزنی اومدم!
-
پل معلق در دل دره «خیاو چایی» اردبیل
-
معاون وزیر کشور: پیشنویس لایحه افزایش تعداد نمایندگان مجلس تهیه شد
-
دورتموند با کواچ تمدید کرد
-
مرسدسبنز از خیر سرمایهگذاری در نیسان گذشت
-
حدادی: اوریه احتمالا از بازی بعدی با ماست
-
شمارش معکوس افزایش ظرفیت تأمین آب تهران
سایر اخبار مرتبط
نظرات
ثبت نظر
مهمترین اخبار

شمارش معکوس افزایش ظرفیت تأمین آب تهران
سهشنبه 05 شهریور 1404 - 14:50:29

رکوردشکنی همراه مکانیک در 1403 به روایت آمار
سهشنبه 05 شهریور 1404 - 14:36:18

کدام شرکتها سود سهام عدالت را واریز نکردند؟
سهشنبه 05 شهریور 1404 - 14:24:20

ادامه ریزش قیمت ارزهای معتبر در مرکز مبادله ایران
سهشنبه 05 شهریور 1404 - 14:22:22

جزئیات وامهای قرضالحسنه اعلام شد
سهشنبه 05 شهریور 1404 - 14:18:00



